
近日,华东师大生命科学学院
杨嘉龙团队研究成果
揭示T细胞免疫的进化规律,
被选为Advanced Science的卷首文章
科研团队请来本校美术学院博士生贾点墨
绘制了一张图《鲤鱼跃龙门》
来解释这个科研发现——
在硬骨鱼(鲤鱼)进化(跃龙门)为
四足动物(龙)的过程中
T细胞免疫基本不变
保守的谷氨酰胺(分子式)代谢途径
为这种稳定进化奠定了分子基础
这张图,你读懂了么?
也可以继续往下看专业解读——
伴随生命的演化,免疫系统日趋复杂。
4.5亿年前,鱼类率先衍生出基于T、B细胞的适应性免疫系统;这种体系在漫长的进化中被继承和发扬,成为四足动物免疫防御的准则。然而,比较基因组学的证据显示,适应性免疫的左膀(T细胞)和右臂(B细胞),似乎经历了截然不同的进化模式。
B细胞免疫随着物种的演化而逐步完善,这不仅体现在新型免疫球蛋白、生发中心的依次出现,更体现在抗体亲和力成熟、类型转换等机制的相继获得。相比之下,T细胞的种类及核心组件,在硬骨鱼向四足动物进化的过程中却基本保持一致。
回顾4.5亿年的进化历程,自然选择的压力造成了五次物种大灭绝,使得四足动物与鱼类在免疫器官、生存环境、膳食结构等方面产生了巨大变化。
为应对这些挑战,B细胞免疫的进化与完善并不难以理解,而T细胞免疫的稳定遗传则显得愈发神秘。
图片研究团队:杨嘉龙教授、博士研究生李康、硕士研究生焦新迎、韦秀梅副教授
研究团队以罗非鱼、非洲爪蟾、鸡、小鼠等动物为研究对象,试图回答两个科学问题:
(1)比较基因组层面的T细胞稳定进化假说,是否体现在免疫学过程、功能和调控机制上?
(2)维持T细胞免疫稳定进化的潜在驱动力是什么?
研究团队首先以低等脊椎动物罗非鱼为模型,描绘了早期T细胞免疫的概况。罗非鱼T细胞通过动态增殖和凋亡,形成了典型的初次、记忆免疫应答;鱼类T细胞的完全活化依赖第一、第二信号的协同作用,并由Ca2+-NFAT、MAPK/ERK、NF-kB和mTORC1通路共同调节;选择性耗竭模型表明IgM+B细胞可向T细胞递呈抗原,确保T细胞的活化和增殖。在功能上,鱼类T细胞具备特异性杀伤靶细胞的细胞毒性功能,并可辅助IgM+B细胞的增殖和抗体分泌。这些结果表明,T细胞免疫的核心策略早在硬骨鱼中即已确立。

谷氨酰胺代谢调控硬骨鱼和四足动物T细胞免疫
为了解析鱼类T细胞免疫的调控机制,研究团队进行了转录组学分析。结果显示,罗非鱼使用了与哺乳动物相似的转录调控网络支持T细胞免疫;而病原感染罗非鱼后,T细胞的差异表达基因主要富集于代谢通路,且发生了大规模的代谢重编程。由于重编程的代谢程序均直接或间接溯源至谷氨酰胺分解代谢,进而探讨了谷氨酰胺代谢对罗非鱼T细胞免疫的调控。活化的罗非鱼T细胞增加了谷氨酰胺的利用;而谷氨酰胺剥夺或谷氨酰胺酶GLS1的抑制,造成了T细胞增殖和效应功能的障碍。进一步的研究证实,mTORC1和MAPK/ERK通路承接了TCR信号,通过c-Myc调控谷氨酰胺代谢,并促进罗非鱼T细胞免疫。
基于罗非鱼与哺乳动物在T细胞代谢及重编程方面的相似性,研究团队猜测:谷氨酰胺代谢调控T细胞免疫可能是有颌脊椎动物进化中的保守策略。
为了验证这一猜测,研究团队选取不同进化阶段的脊椎动物,分析了谷氨酰胺代谢与T细胞免疫的关联。
结果表明,罗非鱼、非洲爪蟾、鸡和小鼠共享了保守的c-Myc驱动谷氨酰胺代谢以调控T细胞免疫的机制。此外,c-Myc或GLS1的敲降损害了人类JurkatT细胞的激活和增殖,而使用罗非鱼的相应分子重建谷氨酰胺代谢途径,能够挽救人类T细胞的免疫缺陷。该发现为理解T细胞免疫的进化提供了新视角,也为干预人类免疫缺陷提供了潜在途径。
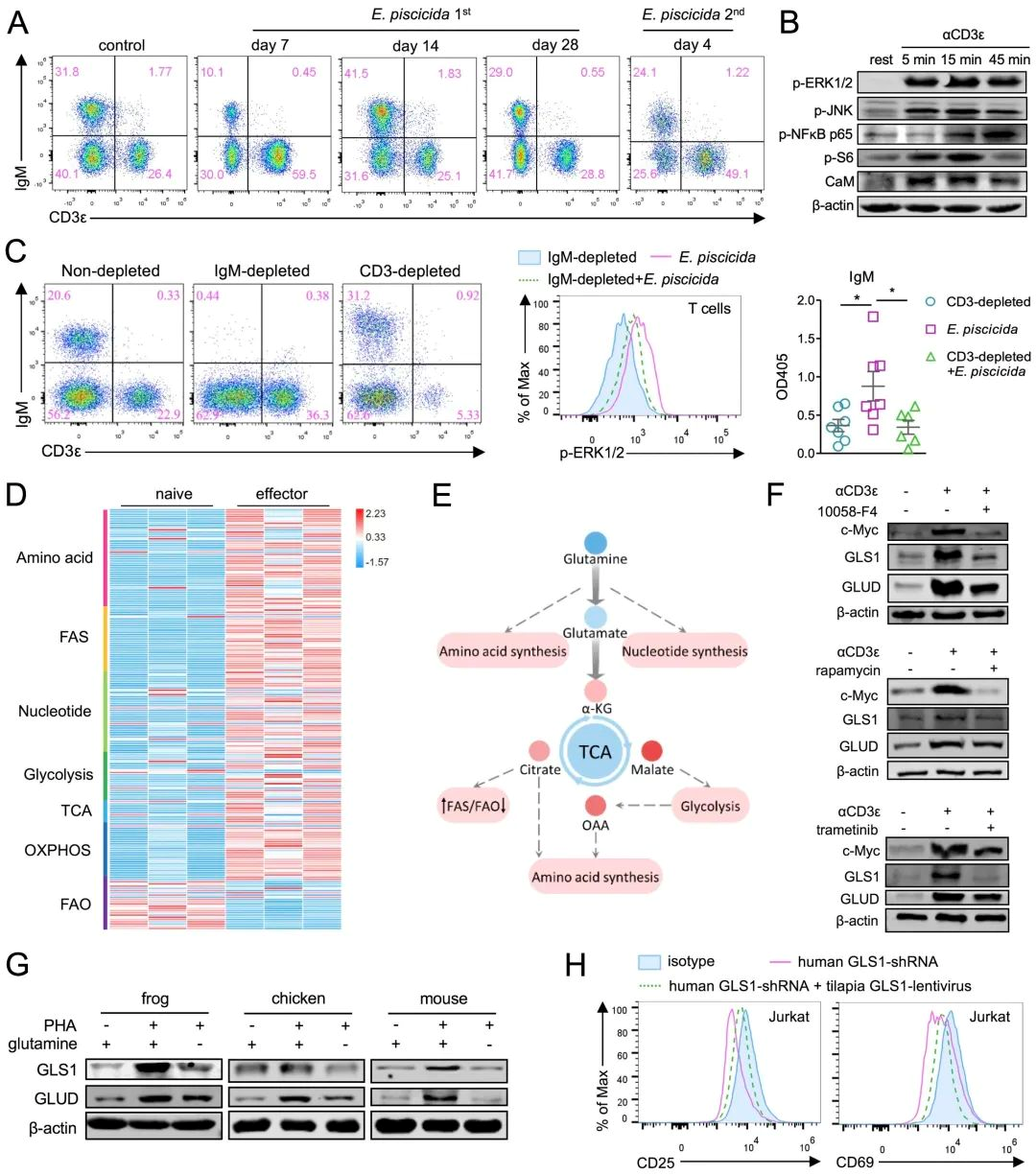
谷氨酰胺代谢是硬骨鱼和四足动物之间T细胞功能相似性的分子基础
综上所述,该研究验证了T细胞免疫稳定进化的假说,并提出保守的转录调控网络和代谢程序,尤其是谷氨酰胺分解代谢,是硬骨鱼与四足动物之间T细胞功能相似性的分子基础。
华东师大生命科学学院博士研究生李康、韦秀梅副教授、硕士研究生焦新迎,和温州医科大学邓文海博士为本文的共同第一作者,华东师大杨嘉龙教授为本文通讯作者。该研究受到国家自然科学基金优秀青年科学基金项目、面上项目等资助。